Принципы применения ПМС: выбор препарата, дозы и методы введения; оценка эффекта и смена препарата
Смотри еще: Антибиотико- и химиотерапия инфекций у детей (В.К. Таточенко, Москва, 2008), Антибиотики у детей (В.К. Таточенко, Москва, 2008).
Выбор препарата, дозы и методы введения
Основной принцип применения ПМС — его соответствие целевому микроорганизму.
Антибиотики эффективны только при бактериальных инфекциях; их применение при ОРВИ и ОКИ (что, к сожалению, наблюдается часто) лишь повышает риск побочных явлений и развития устойчивости флоры.
Не получив эффекта в такой ситуации, врач теряет веру в назначенный препарат и переходит на резервные препараты. То же происходит и при применении противовирусных средств в поздние сроки инфекции, хотя они эффективны лишь в фазе репликации вирусов в первые 1-2 дня.
Поэтому вопрос о том, показаны ли ПМС данному больному — важнейший. Врач может назначить ПМС при неполной информации о болезни, особенно тяжелой; важно, однако, чтобы по получении проясняющих диагноз данных коррегировать назначение или отменить ПМС, если оно не показано. При выборе ПМС важен учет не только характера возбудителя, но и факторов пациента.
В педиатрии к факторам пациента относится, прежде всего, его возраст, поскольку спектр возбудителей меняется, в т.ч. вследствие естественной иммунизации. У детей важны учет аллергических проявлений, оценка функции печени и почек. Учет фактора возбудителя предусматривает определение вероятных возбудителей и их чувствительность к ПМС. При выделении возбудителя из стерильных в норме сред (кровь, СМЖ, экссудат) это несложно — такая терапия называется целенаправленной. Но и в отсутствие высева можно со значительной долей вероятности «вычислить» возможных возбудителей и подобрать эффективные ПМС (с учетом локальной резистентности возбудителей) для стартовой эмпирической терапии, как это обычно бывает при острых инфекциях (до начала ее проведения желательно получить образцы для посева).
Монотерапия ПМС узкого спектра предпочтительна, комбинации препаратов имеют целью расширение антибактериального спектра (особенно при отсутствии данных о возбудителе), а также для предотвращения (например, при туберкулезе) лекарственной устойчивости. Синергизм наблюдается у препаратов, действующих на разный субстрат бактериальной клетки. Применение более 2 препаратов практикуется при туберкулезе и у больных при пересадке костного мозга или стволовых клеток.
Препараты 1-го выбора используют при внебольничных инфекциях, когда нет оснований предполагать наличие лекарственной устойчивости. При предшествующей (за 1-3 месяца) терапии антибиотиками, а также при внутрибольничной инфекции, следует начинать с препаратов 2-го выбора. Средства 3-го выбора (резервные) применяют только в случаях полирезистентности.
Выбор дозы
Высокие дозы показаны при более тяжелых процессах, а также при сниженной чувствительности возбудителя к препарату; назначение ПМС в «стандартной», а не в максимальной дозе может снизить эффективность лечения. Высокие дозы требуются и прилечении менингита, т.к. переход препарата в СМЖ зависит от пика его концентрации в крови. Но применять дозы выше максимально рекомендованных не следует, лучше использовать другой препарат, к которому возбудитель более чувствителен.
Эффективный и безопасный диапазон доз ПМС указывается в инструкциях к препарату, однако, в наставлениях к ряду ПМС изготовители рекомендуют низкие «обычные дозы», которые, хотя и эффективны в ряде случаев, в других «обычных» случаях оказываются недостаточными. Поэтому рекомендации этого руководства могут отличаться от наставлений.
Общепринято дозирование ПМС по весу, но для некоторых препаратов указываются дозировки по площади поверхности тела. В Табл. 1.1. приведены данные, позволяющие легко провести необходим пересчет.
При лечении детей с избыточным весом выбор дозирование лучше вести на стандартный вес для данного роста, взятый из таблиц вес-рост.
Табл. 1.1 Дозирование по поверхности тела у детей
| Вес в кг | Площадь м2 | % дозы взрослого |
| 3,5 | 0,22 | 13 |
| 7 | 0,35 | 20 |
| 10 | 0,45 | 30 |
| 15 | 0,65 | 40 |
| 20 | 0,80 | 45 |
| 25 | 0,95 | 55 |
| 30 | 1,05 | 65 |
| 40 | 1,25 | 75 |
| 50 | 1,50 | 90 |
| 70 | 1,70 | 100 |
Пути введения
У детей основным путем введения ПМС является оральный как наименее травматичный. Из оральных детских форм (сиропы, суспензии, растворимые гранулы и таблетки) предпочтительны средства, допускающие точность дозировки, не содержащие сахара и не вызывающие аллергических реакций. Важно пользоваться прилагаемой мерной ложкой, поскольку современные чайные ложки редко вмещают 5 мл. Более точно дозируются растворимые гранулы, а также — диспергируемые таблетки (например, типа Солютаб — Флемоксин, Флемоклав, Вильпрафен, Юнидокс).
Из парентеральных путей более приемлем внутривенный: при наличии периферического венозного катетера он менее травматичен, чем внутримышечный. После наступления эффекта от лечения следует перейти на оральный препарат (ступенчатый метод).
Аэрозольный путь используется лишь при длительной терапии муковисцидоза (плохое проникновение в очаг поражения в легком). Эндобронхиальное введение используют в начале лечения гнойных процессов.
Разовые дозы и кратность введения
Дозы и кратность введения должны быть достаточны для обеспечения бактерицидного действия препарата в месте его приложения. Рекомендации о 4-, 6- и 8-кратном введении антибиотиков на заре их применения были связаны с использованием низких доз; они привели к настоящей инъекционной эпидемии. Так, в/м введение 2 антибиотиков 4 раза в день в разных шприцах, например, при пневмонии требовало 50-60 инъекций на курс лечения. ВОЗ описан ребенок в Румынии, получивший в первые месяцы жизни 500 в/м инъекций.
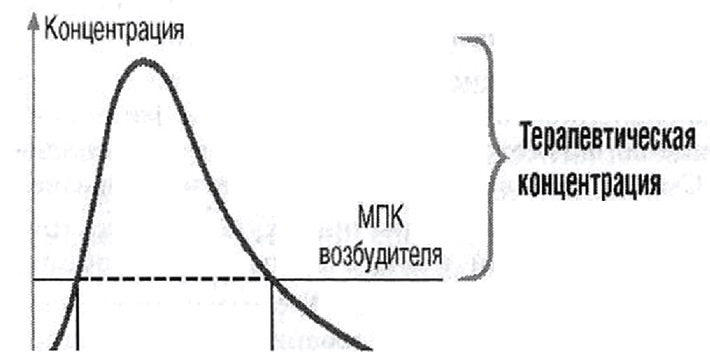
Повышение разовой дозы антибиотика сопровождается усилением перехода его в ткани. Для пенициллинов, цефалоспоринов, карбапенемов и макролидов важно, чтобы их концентрация в тканях превышала минимальную подавляющую (МПК) для данного возбудителя в течение 45-50% времени (Рис. 1.1.); повышение концентрации не усиливает их бактерицидность.
Рис.1.1. Концентрация лактамов и макролидов должна превышать МПК возбудителя в течение 45-50% времени
Снижение концентрации ПМС в тканях происходит намного медленнее, чем в сыворотке, поэтому повышение разовой дозы (при той же суточной) обеспечивает требуемую концентрацию ПМС в тканях в течение 8-12 часов и более. В среднем, доза ПМС должна давать пик концентрации в крови, превышающий МПК возбудителя в 4-8 раз.
Как показали контролируемые клинические испытания, сокращение кратности введения бета-лактамов (пенициллины, цефалоспорины) до 2-3 раз в сутки (при тех же суточных дозах) не снижает, а часто повышает эффективность лечения. Рекомендуемые сейчас их суточные дозы при 2-кратном введении создают в тканях концентрации, которые остаются выше МПК в течение 8-10 часов и более, что достаточно для получения клинического и бактериологического эффектов.
Бактерицидность аминогликозидов, метронидазола и фторхинолонов, напротив, пропорциональна их пиковой концентрации в тканях; с учетом длительного постантибиотического эффекта этих препаратов их лучше вводить 2 и даже 1 раз в сутки. Такая тактика безопасна, поскольку токсичность (в частности, ототоксичность) зависит от величины средней концентрации, т.е. от суточной дозы. Один раз в день вводят также азитромицин, рифампицин и цефтриаксон.
Наши рекомендации по более редкому введению антибиотиков приняты во многих клиниках, в т.ч. и в других странах. Большинство современных рекомендаций содержат указания о 2-3-кратном введении бета-лактамных препаратов, макролидов и 1-2-кратном — аминогликозидов. И только при сепсисе важно постоянство концентрации антибиотика в крови, которое достигается 4-кратным или капельным его введением.
Оценка эффекта и смена препарата
Продолжать лечение стартовым препаратом есть смысл только при наступления эффекта, который при остром заболевании наступает через 36-48 часов от его начала.
Полный эффект — падение температуры ниже 38°, улучшение состояния, уменьшение изменений в очаге — указывает на чувствительность возбудителя к препарату.
Частичный эффект — сохранение фебрильной температуры при снижении степени токсикоза, одышки, улучшении аппетита — в отсутствие отрицательной динамики в очаге воспаления (распространения процесса). Частичная эффективность антибиотиков наблюдается обычно при образовании гнойника, она связана со снижением кровотока и фагоцитарной функции. Гной также уменьшает активность аминогликозидов, макролидов, линкозамидов из-за снижения рН среды и/или усиленного связывания антибиотика с продуктами распада тканей. Улучшение достигается опорожнением гнойника.
Другая причина частичного эффекта — метаинфекционная лихорадка, связанная с образованием иммунных комплексов и воспалением в шоковом органе (см. метапневмонический плеврит в Главе 2). Ее подавление возможно с помощью противовоспалительных средств (стероидов или НПВС). Смена ПМС в обоих случаях нецелесообразна.
Отсутствие эффекта — сохранение фебрильной температуры при ухудшении состояния и/или распространении патологических изменений в очаге воспаления и общих расстройств (одышки, гипоксемии и др.) — требует смены антибиотика.
После получения результатов микробиологического исследования возможна коррекция противомикробной терапии. При получении отрицательного результата посева вопрос о продолжении или смене ПМС решается на основании клинических данных. Следует учитывать, что при тяжелых инфекциях отсутствие клинического эффекта может быть не связано с неэффективностью этиотропной терапии.
Длительность терапии
Оптимальная длительность терапии должна быть достаточной для того, чтобы подавить возбудителя и позволить иммунологическим механизмам закончить его элиминацию или инактивацию. При многих процессах оптимальная длительность лечения установлена экспериментально с учетом как непосредственного эффекта, так и риска развития клинического и/или бактериологического рецидива. При острых инфекциях антибиотики вводят в течение минимум 2 дней после нормализации температуры и стихания признаков острого воспаления (исчезновение болей, отхождения экссудата и т.д.). После появления эффекта лечения следует перейти на оральные препараты.
Определяя длительность лечения, не следует ориентироваться на полную нормализацию изменений; такие симптомы как гиперсекреция слизи в дыхательных путях, уплотнение подкожной клетчатки в месте воспаления, рентгенологические изменения при пневмонии и др. сохраняются значительно дольше, чем активное микробное воспаление. С другой стороны, при сепсисе, эндокардите и других тяжелых процессах рекомендуются длительные курсы терапии, захватывающие период полного отсутствия симптомов, что необходимо для ликвидации тлеющего очага инфекции. При лечении хронических процессов приходится ориентироваться и на параклинические признаки активности.
Использование принципов доказательной медицины при выборе ПМС
При выборе ПМС, как и любого другого лекарственного средства, следует учитывать не только и не столько сложившийся стереотип его использования, сколько результаты рандомизированных контролируемых испытаний, проведенных в соответствии со стандартами доказательной медицины. Такие данные имеются в отношении многих инфекций, появление новых ПМС сопровождается постоянной переоценкой схем терапии, имеющей целью ее оптимизацию. Приведенные нами материалы по выбору ПМС сделаны с учетом последних рекомендаций наиболее авторитетных групп исследователей как в России, так и за рубежом, а также данных метаанализа клинических испытаний. В отсутствие рекомендаций мы ссылаемся на данные отдельных исследований или мнения экспертов — это становится ясным из текста и сносок. Мы учитывали и данные о резистентности возбудителей в России.
Смотри еще: Антибиотико- и химиотерапия инфекций у детей (В.К. Таточенко, Москва, 2008), Антибиотики у детей (В.К. Таточенко, Москва, 2008).