Инфаркт нижней стенки у пациента с COVID-19 (случай на Диагностере)
Пациент, 55 лет, в течение трех дней жалуется на лихорадку и боли за грудиной.
Наблюдается по поводу гипертонической болезни, дислипидемии, хронической обструктивной болезни легких.
Контакте с инфицированным COVID-19 неделю назад.
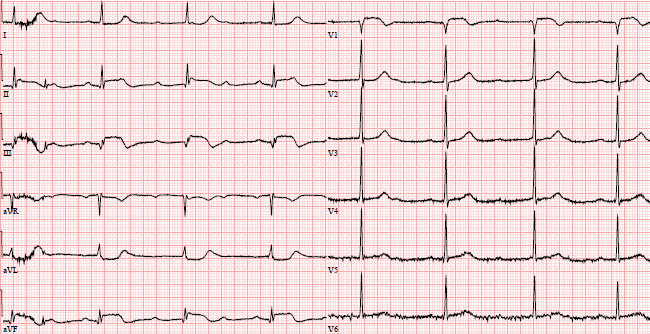
На ЭКГ выявлены признаки нижнего инфаркта миокарда на фоне АВ-блокады III типа.
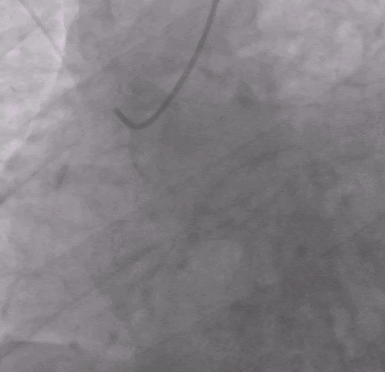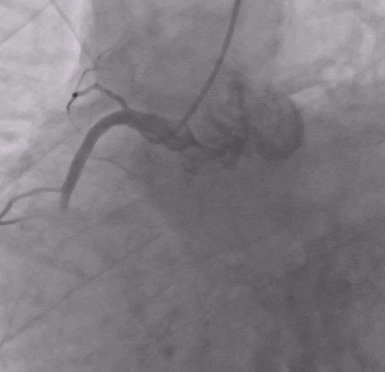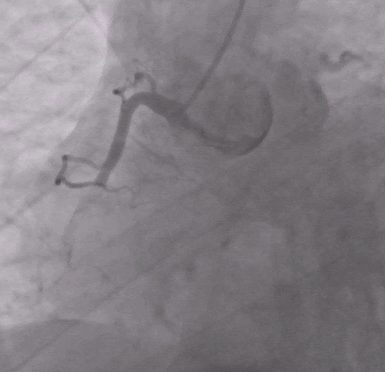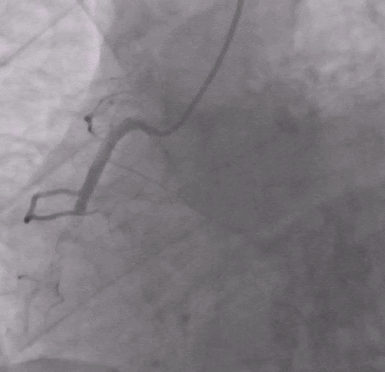
Экстренная селективная коронарография: выявлена тромботическая облитерация средней части правой коронарной артерии (ПКА).
После извлечения тромба и введения эптифибатида было выполнено ЧКВ с имплантацией стента.
После ЧКВ синусовый ритм восстановился, и все оставшиеся клинические симптомы были связаны с двусторонней пневмонией.
COVID-19 (подтвержденной с помощью ПЦР) с подозрением на бактериальную суперинфекцию (CRP 268 мг / л, лейкоцитоз 22,8 · 10 ^ 9 / л).
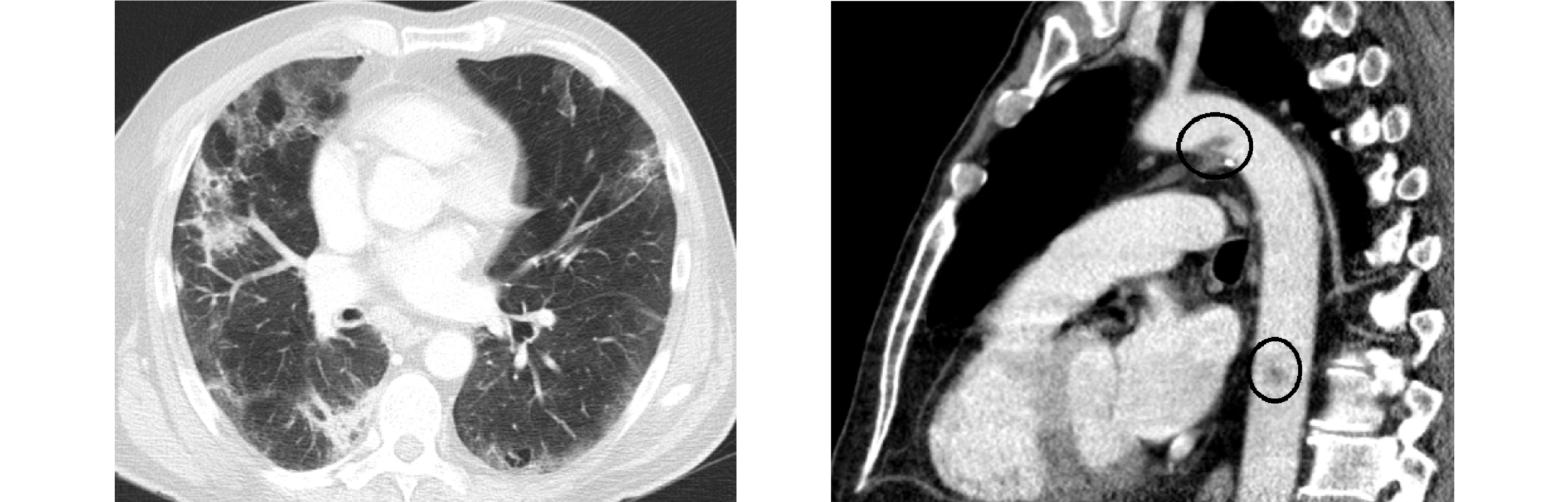
КТ грудной клетки показала двустороннюю пневмонию с возможными постпневмоническими изменениями на месте хронической эмфиземой.
КТ-ангиография исключила тромбоэмболию легочной артерии (ТЭЛА), но были обнаружены тромбы в нисходящей аорте и дуге аорты.
Это тромботическое осложнение, скорее всего, было связано с состоянием гиперкоагуляции, вызванным инфекцией SARS-CoV-2.
Начата эмпирическая терапия АТБ левофлоксацин + цефотаксим, начата антикоагулянтная терапия.
Состояние пациента быстро улучшилось в течение следующих нескольких дней и стабилизировалось на неинвазивной кислородной терапии.
Выводы
Есть неопровержимые доказательства того, что у пациентов с COVID-19 существует значительный риск тромбоза.
Коагулопатия сообщается почти у 50% пациентов с тяжелыми проявлениями COVID-19.
Наиболее значительным изменением параметров коагуляции является увеличение D-димеров, и постепенно увеличивающиеся значения могут использоваться в качестве прогностического параметра.
Наиболее частые тромботические осложнения включают тромбоэмболию легочной артерии (ТЭЛА) или тромбоз легочной артерии (ТГ), тромбоз глубоких вен (ТГВ), ишемический инсульт, инфаркт миокарда и системную артериальную эмболию.
Вирус SARS-CoV-2 связан с гиперкоагуляционным состоянием, которое характеризуется нарушениями в тестах свертывания (PT и APTT), повышенными D-димерами и повышенным тромботическим статусом.
Гиперкоагуляция вызывается несколькими факторами: включает прямое взаимодействие вируса с определенными тканями и тромбоцитами, воспаление, активацию комплемента и неэффективный тромболизис.
Тем не менее, пока неизвестно, являются ли эти гемостатические изменения специфическим эффектом SARS-CoV-2 или следствием цитокинового шторма, который ускоряет начало SIRS, как это наблюдается при других вирусных заболеваниях.
Предлагаемые механизмы иммунотромбоза при COVID-19 и взаимодействия систем воспаления и свертывания.
Прямое взаимодействие SARS-CoV-2 — тромбоциты приводит к высокому уровню активации тромбоцитов, способствуя протромботическому состоянию.
Результат гиперкоагуляционного состояния, вызванного SARS-CoV-2, показывает специфическое повреждение, которое не типично для других подобных вирусных инфекций.
Легочный микротромбоз — при ультразвуковом вскрытии тромбы фибрина в легочных артериолах были обнаружены в 8 случаях из 10.
Это указывает на первичный тромбоз легких, который, скорее всего, вызывает типичное быстрое развитие гипоксемии на ранних стадиях ОРДС у пациентов с COVID-19.
Микротромбы создают несоответствие вентиляции / перфузии и последующее увеличение мертвого пространства.
Легочный тромбоз, а не эмболия. Диагностика тромбоэмболии легочной артерии является наиболее частым исходом гиперкоагуляционного состояния у пациентов с COVID-19, и кажется, что во многих случаях ЛТ не всегда предшествует тромбоз глубоких вен (ТГВ) и, скорее всего, происходит главным образом из-за легкие.
Это согласуется с данными о микротромбозе легких и имеет два практических последствия.
1) обычно используемые критерии Уэла для ТЭ, зависящие от наличия симптомов ТГВ, больше не являются релевантной системой подсчета баллов и 2) ЛТ имеет другие патогенетические механизмы, чем ТЭ, и может изменять рекомендации по лечению.
Стандартной профилактической терапии НМГ может быть недостаточно для предотвращения легочных тромботических осложнений.
Распространенное внутрисосудистое свертывание крови — заболеваемость ДВС-синдромом была зарегистрирована у 2,2% госпитализированных пациентов, однако 71,4% неживых соответствует критериям ДВС-синдрома Международного общества тромбоза и гемостаза (ISTH) (которые включают количество тромбоцитов, фибриноген, D- Димерное и протромбиновое время) по сравнению с 0,6% выживших.
Таким образом, наличие симптомов ДВС-синдрома может быть полезным прогностическим инструментом.
Коагулопатия при COVID-19 отличается от ДВС-синдрома по другим причинам.
У пациентов наблюдается явное отсутствие кровотечений, только умеренное удлинение АЧТВ, повышенный фибриноген и отсутствие шистоцитов в мазке крови.
Есть несколько теорий, объясняющих это, от локализованного легочного внутрисосудистого свертывания, происходящего из-за взаимодействия рецептора ACE2 эндотелиальных клеток с SARS-CoV-2, до опосредованной комплементом тромботической микроангиопатии с дополнительным наличием анемии, повышением уровня ЛДГ и почечной дисфункцией.
Сердечно-сосудистые осложнения — острое повреждение сердца наблюдается у 7–28% госпитализированных пациентов и связано с повышенным риском тяжелого заболевания и смерти.
Это может происходить из-за вирус-опосредованного лизиса кардиомиоцитов (что наблюдается при других вирусных инфекциях) или из-за связывания с рецепторами ACE2 в сердце.
Когда вирус связывается с рецепторами ACE2, активность ACE2 снижается и может уменьшать кардиозащитные эффекты фермента.
У многих пациентов подозревали миокардит, но частота его возникновения неизвестна из-за неполных гистологических исследований.
Нестабильность атеросклеротической бляшки — воспаление и высвобождение цитокинов увеличивают миграцию воспалительных клеток и инфильтрацию бляшки, что может привести к нестабильности бляшки с последующим образованием артериальных тромбов.
Разрыв атеросклеротической бляшки может привести к коронарному тромбозу и острому инфаркту миокарда.
В целом, у пациентов с факторами риска атеросклероза, такими как артериальная гипертензия и диабет, вероятность развития тяжелых симптомов, требующих госпитализации в ОИТ, в 2-3 раза выше.
