Случай: лечение гигантоклеточного миокардита
Женщина в возрасте 64 года; после обморока впервые выявлена АВ-блокада третьей степени.
Тропонин Т 1086 нг/л (N 0-14 нг/л), натрийуретический пептид типа В 2164 нг/л (N 10-155 нг/л).
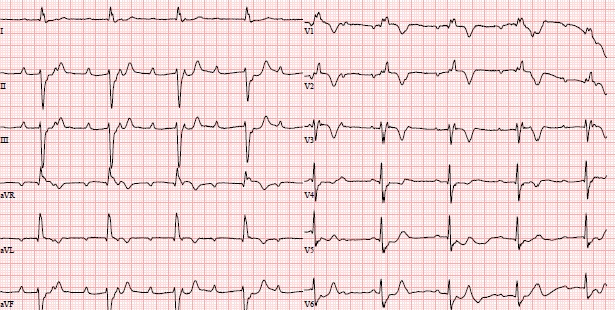
На ЭКГ синусовый ритм, полная АВ-блокада; суточное ЭКГ по Холтеру выявило паузы до 5 сек.
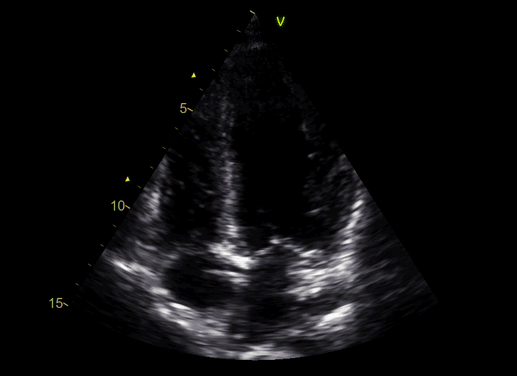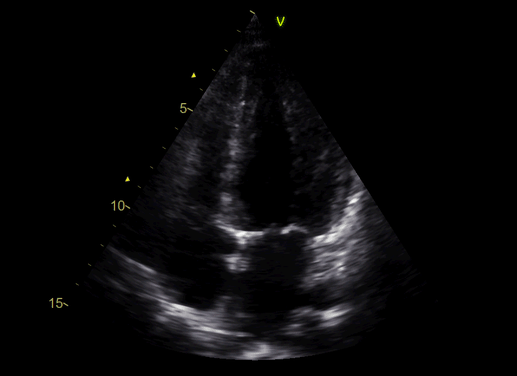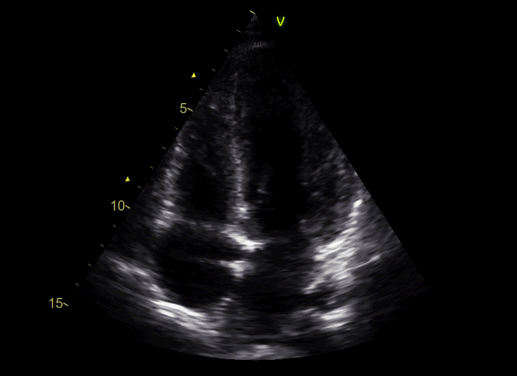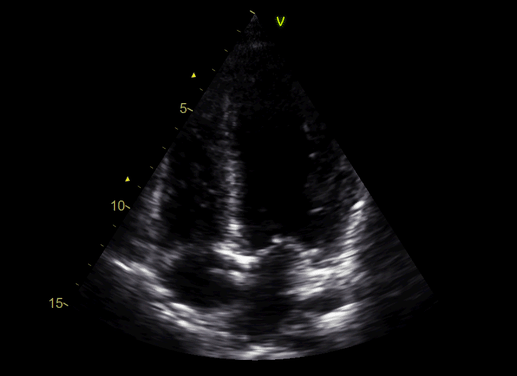
На ЭхоКГ фракция выброса ЛЖ пограничная (50%), а коронарография без значимой патологии.
На 2-ой день установлен временный водитель ритма, выполнена эндомиокардиальная биопсия.
На 4-ый день фракция выброса ЛЖ снижена до 30-35%; внедрен постоянный кардиостимулятор.
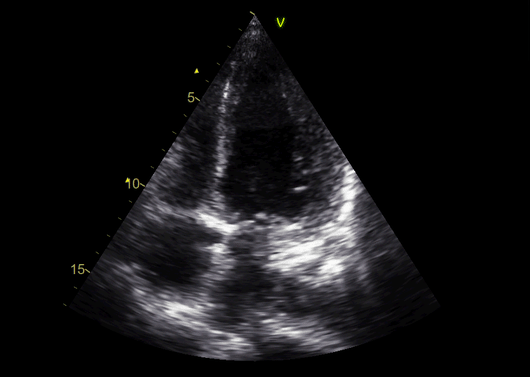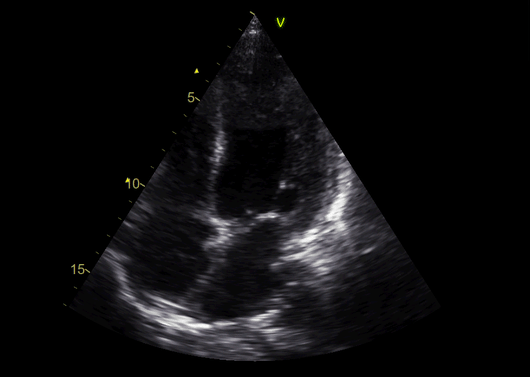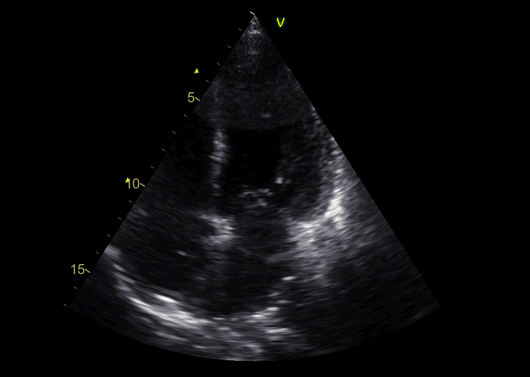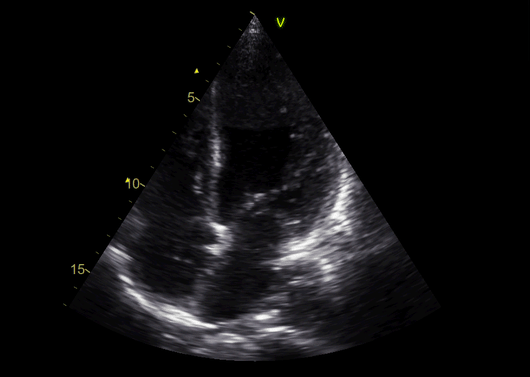
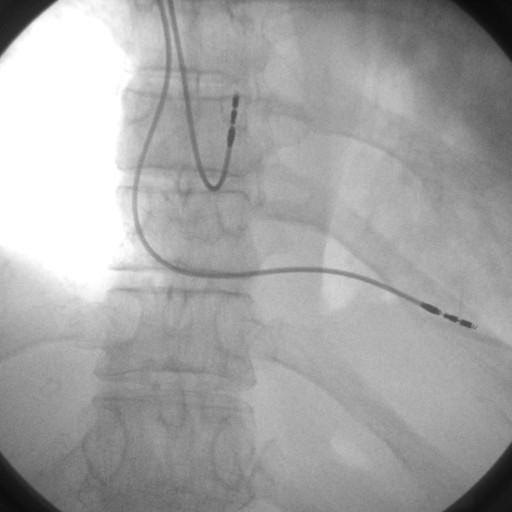
Дальнейшее прогрессирование систолической дисфункции ЛЖ, требующее введения левосимендана, наблюдалось в течение следующих 2 дней, и пациенту была показана эндомиокардиальная биопсия (ЭМБ).
Биопсия эндомиокарда выявила диффузную воспалительную целлюлизацию с обширным разрушением тканей и наличием гигантских многоядерных клеток.
Рассмотрена возможность комбинированной иммуносупрессивной терапии.
Однако из-за развития внутрибольничного сепсиса неизвестного происхождения (С-реактивный белок, 231 мг / л [нормальный диапазон, 0-5 мг / л]; прокальцитонин, 2,56 мкг / л [нормальный диапазон, 0-0,5 мкг / л] ]) было начато лечение только 60 мг преднизона.
Однако дальнейшее прогрессирование низкого сердечного выброса с непрекращающейся желудочковой тахикардией потребовало острой имплантации вспомогательного устройства для левого желудочка (LVAD) (Levitronix CentriMag, Waltham, MA) на восьмой день после госпитализации.
Поскольку восстановления не наблюдалось, долгосрочный LVAD (Heart Mate II, Thoratec, Pleasanton, CA) был имплантирован на 17-й день после госпитализации в качестве моста к трансплантации.
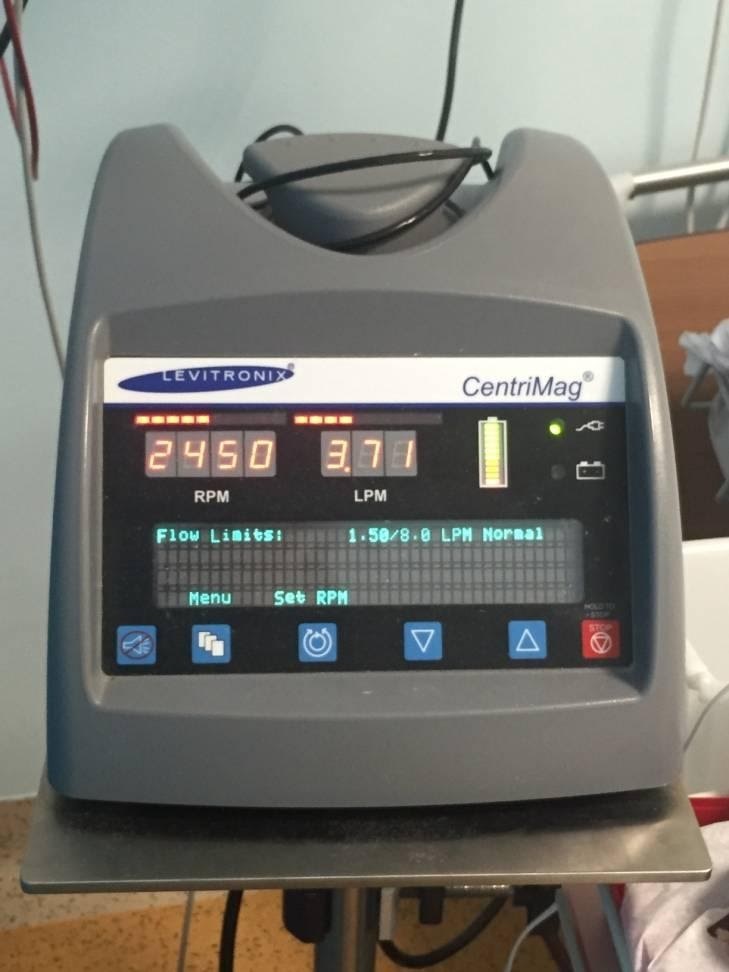
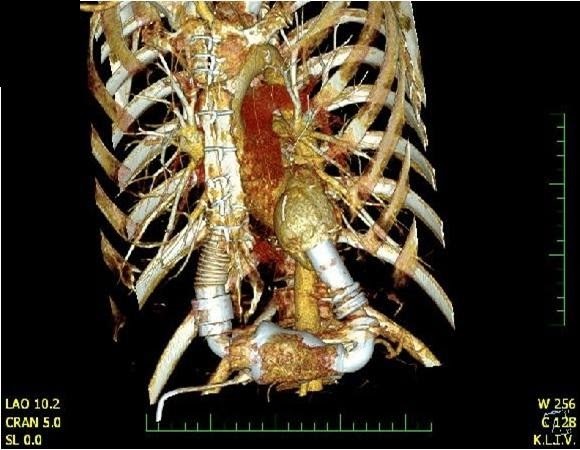
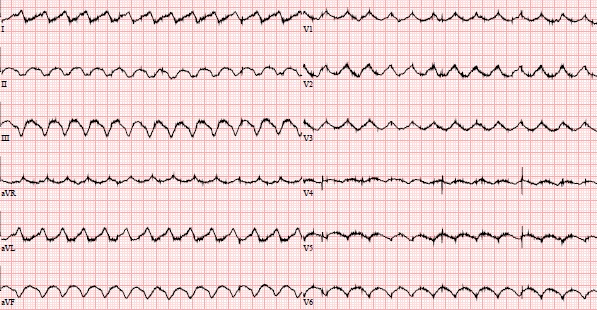
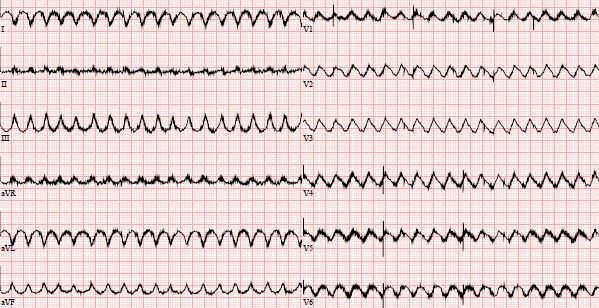
Через пять недель после имплантации LVAD произошел электрический шторм, вызванный плеоморфными желудочковыми аритмиями, которые стали устойчивыми к антиаритмической терапии амиодароном.
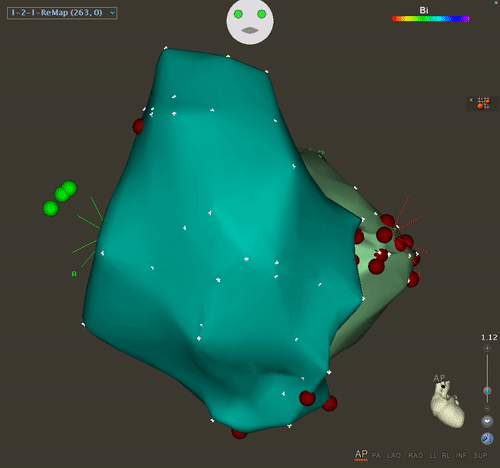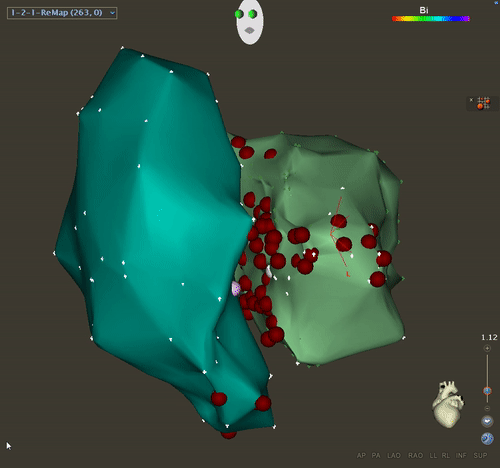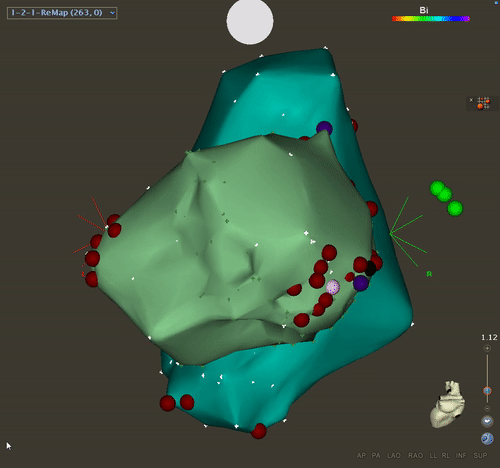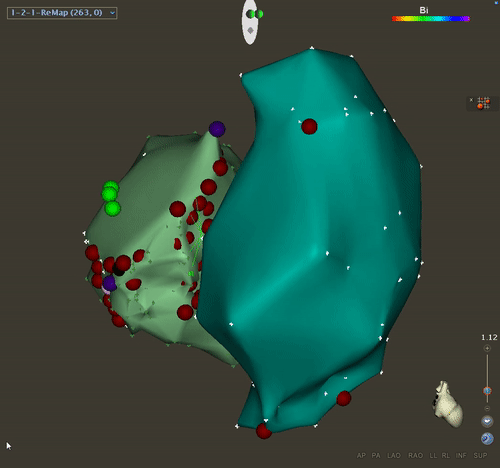
Поэтому на 60-е сутки после поступления была выполнена радиочастотная катетерная аблация из транссептального доступа.
Существенная модификация субстрата была выполнена путем нанесения повреждений вдоль перегородки и вокруг митрального кольца.
Катетерная аблация была успешной в предотвращении рецидивов желудочковых аритмий.
Впоследствии пациентка была внесена в список срочных кандидатов на трансплантацию сердца.
Однако клиническое течение осложнялось развитием тяжелой аортальной регургитации, которой не было на момент имплантации LVAD.
Транскатетерная имплантация аортального клапана была выполнена на 138-й день после поступления с использованием трансфеморального доступа (EvolutR, 23 мм; Medtronic, Миннеаполис, Миннесота).
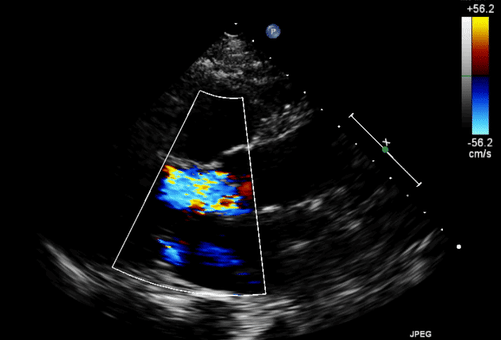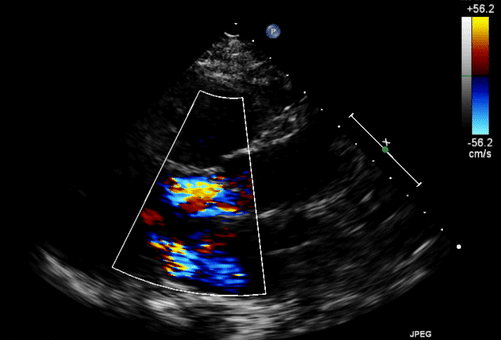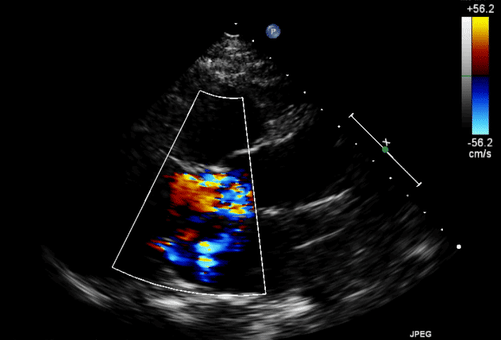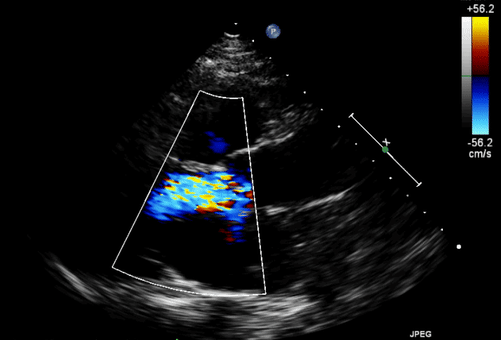
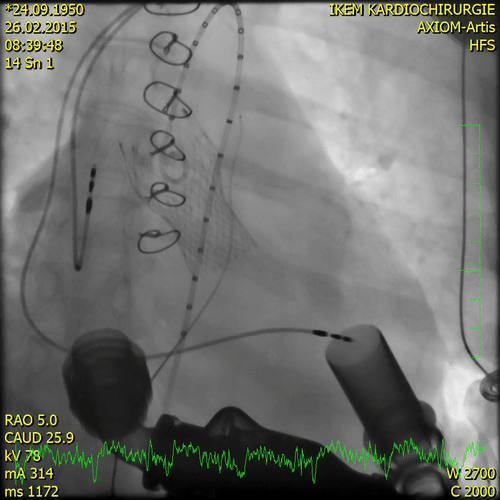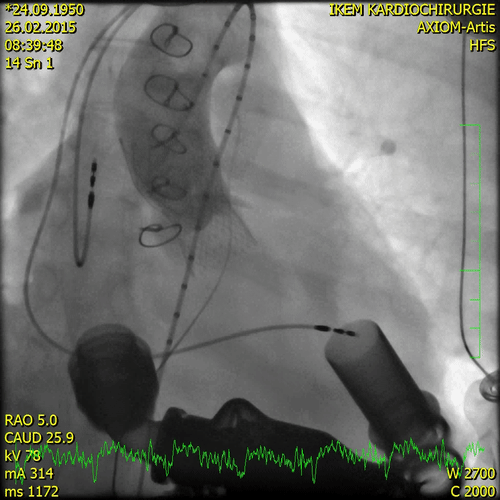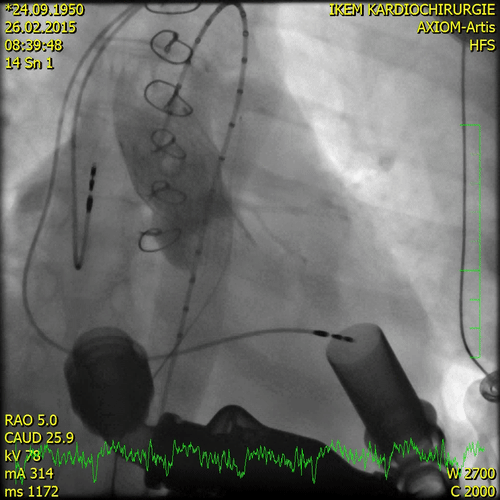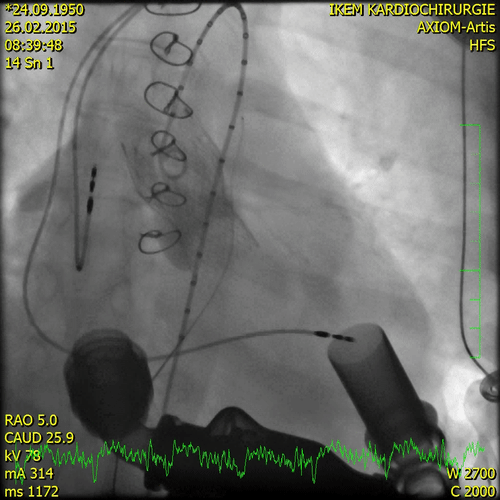
Через шесть месяцев после первичного проявления фульминантного миокардита пациенту была проведена ортотопическая бикавальная трансплантация сердца.
После операции было выполнено 7 процедур эндомиокардиальной биопсии; ни у одного из них не было признаков отторжения или рецидива гигантоклеточного миокардита.
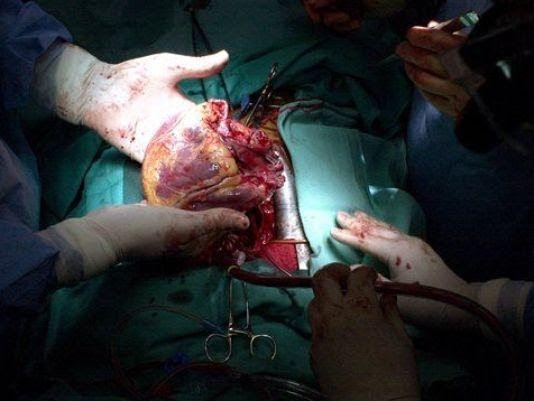
Выводы
1) Тройной иммуносупрессивный режим не всегда может быть подходящим для пациентов с ГКМ (инфекция, VAD). Ретроспективный обзор 32 пациентов с диагнозом ГКМ в Финляндии в период с 1991 по 2011 год показал, что 2/3 достигли клинической ремиссии на тройной иммуносупрессивной терапии (преднизон, азатиоприн, циклоспорин).
2) Радиочастотная абляция ЖТ может быть процедурой, спасающей жизнь пациентам с ДПА. Каковы триггеры VT после имплантации LVAD? Внутренний рубец миокарда Механическая индукция из канюли левого желудочка Послеоперационное увеличение интервала QTc может произойти после разгрузки желудочка с размещением LVAD. Резекция желудочка и разрезы, связанные с установкой канюли оттока левого желудочка
3) Каковы технические трудности радиочастотной абляции? Необходимость транссептального доступа из-за постоянного закрытия аортального клапана с потенциальным риском последующего шунтирования RL Ограниченная маневренность катетера абляции из-за разгрузки ЛЖ и уменьшения объемов ЛЖ Возможность защемления катетера в приточной канюле с риском повреждения LVAD
4) Регургитацию аорты, вызванную имплантацией VAD, можно успешно лечить с помощью TAVI.
